II.3. Az IKs szerepe a repolarizációs tartalék kialakításában
Állatkísérletes és humán vizsgálatok adatai szerint a késői egyenirányító lassú káliumáram (IKs) kulcsszerepet játszik a szívizom repolarizációs tartalékának kialakításában. Az IKs áramot a KCNQ1, KCNE1 és KCNE2 gének által kódolt KvLQT1 pórusformáló α és szabályozó MinK, MIRP β alegységeket felépítő proteinek alkotta ioncsatornák hozzák létre (2. ábra).
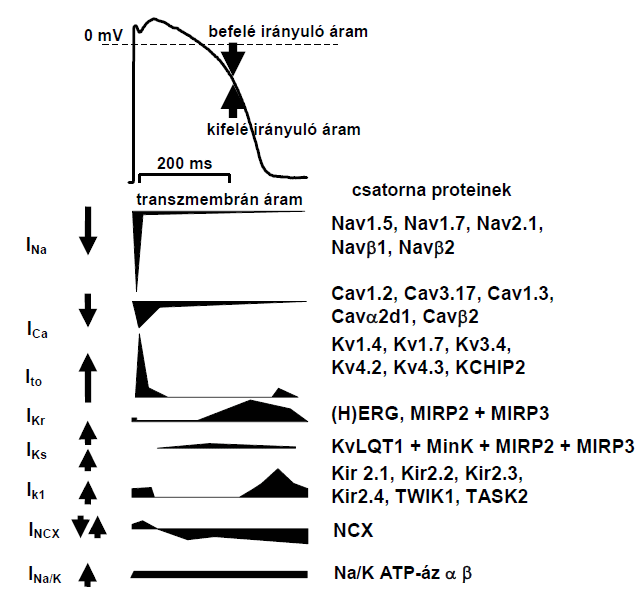
Érdekes és fontos tény, hogy egészséges szívben is az IKs csatornák expressziója regionális és transzmurális eltéréseket mutat. Az IKs áram lassan aktiválódik (500-1000 ms) az akciós potenciál platófázisa alatt, majd gyorsan deaktiválódik (100-200 ms) negatívabb membrán potenciál értékek mellett. Normális körülmények között, az áram kis amplitudója és lassú aktivációs kinetikája miatt viszonylag kevés áram aktiválódik. Ugyanakkor, ha az akciós potenciál időtartama megnyúlik és a platófázis membránpoteciálja pozitívabb értékek irányába tolódik, az IKs egy elérhető tartalék áramot testesít meg, mely szükség szerint nagyobb mértékben aktiválódik. Így az IKs repolarizáló káliumáram egyik legfontosabb szerepe a jelentős akciós potenciál megnyúlás ellensúlyozása. A szimpatikus tónus fokozódása aktiválja az IKs áramot a cAMP/PKA (protein kináz A) út révén. A megnövekedett IKs amplitudó és az aktivációs feszültségtartomány negatívabb tartományba tolódása fokozza az IKs áram denzitását szimpatikus aktiváció során, mely sportolókban sportteljesítmény alatt és azt követően is fennáll. Az L-típusú kalcium áram (ICa,L) szintén fokozódik szimpatikus aktiváció következményeként, a plató fázis alatt a membránpotenciál pozitívabb irányba való eltolódását és a repolarizáció megnyúlását eredményezve. Az IKs áramot ezek a változások még tovább aktiválják és az IKs mintegy negatív feedback mechanizmust hoz létre és így korlátozza a repolarizáció túlzott megnyúlását. Összességében az IKs a repolarizációhoz szignifikánsan járul hozzá a szimpatikus tónus fokozódása, illetve az egyéb repolarizáló káliumáramok (pl. IKr) gátlása révén létrejövő repolarizáció megnyúlása esetén, így ellensúlyozó mechanizmusként működik, mely csak szükség esetén rövidíti az akciós potenciált. Ebből következik, hogy az IKs funkciójának beszűkülése veleszületett okokból (funkcióvesztő mutációk: kongenitális hosszú QT szindróma 1; LQT1), vagy IKs áram gátló gyógyszerek, vagy IKs „downreguláció" következtében (pl. szívizom hypertrophia esetén) súlyosan korlátozza a szívizom repolarizáció megnyúlásra adott válaszkészségét, tehát érzékenyíti a szívizomzatot a repolarizáció zavarainak talaján kialakuló súlyos kamrai ritmuszavarok és a hirtelen szívhalál kialakulására.
Az IKs kritikus szerepén kívül más repolarizáló káliumáramok is hozzájárulhatnak a repolarizációs tartalék kialakításához. Kutya kamrai kísérleti adatok arra utalnak, hogy a tranziens kifelé irányuló káliumáram (Ito) is jelentős tényezője a repolarizációs rezervnek. Ezen felül jelen szerzők kísérleti eredményei bizonyítják, hogy a befelé egyenirányító káliumáram (IK1) gátlása nyulakon és kutyákon a repolarizációs tartalék beszűküléséhez vezetett, valamint a gátlást követően az állatok érzékenysége jelentősen megnőtt a TdP ritmuszavar kialakulására.
Fontos megjegyezni, hogy a legfrissebb eredmények szerint a repolarizációs tartalék nem statikus, hanem dinamikusan változó jelleget mutat. Erre utal többek között, hogy amikor folyamatosan elektromosan ingerelt kutya kamrai szívizomsejtek tenyészetét 24 órán át inkubálták a szelektív IKr gátló dofetiliddel, akkor az akciós potenciál megrövidült, tehát a dofetilid jól ismert akut repolarizációt nyújtó hatását a sejtek fokozatosan ellensúlyozták. A dofetiliddel inkubált sejtekben az IKs csatornák expressziója fokozódott, valamint a patch-clamp technikával mért IKs áram is megnövekedett. Az eredményeket megerősítették az emelkedett KvLQT1 és MinK proteinek szintjei.
A fenti in vitro eredmények megerősítésre várnak in vivo körülmények között, de a fenti eredmények azt sugallják, hogy a szív repolarizáló káliumáramait különböző mértékben gátló szerek krónikus adagolása (pl. bizonyos antibiotikumok, antihisztaminok, egyes gombaellenes szerek, antipszichotikumok, nem-szteroid gyulladáscsökkentők stb.) az IKs csatornák kompenzatorikus „up-regulációját" okozhatják a szívizomzat repolarizációs kapacitásának helyreállítására tett kísérlet részeként. Belátható, hogy ha az IKs funkciója genetikai okok miatt már előzetesen csökkent, (pl. LQT1 szindróma esetén), illetve a csatorna „down-regulációja" következik be (pl. szívizom hypertrophia esetén), látszólag teljesen ártalmatlan gyógyszeres terápia élsportolókban váratlan módon fokozhatja a szívizom repolarizáció zavarait és a következményes súlyos kamrai ritmuszavarok kialakulásának valószínűségét.